Ein Protein als Schlüssel gegen antibiotikaresistente Bakterien
Tübinger Forschende finden ein Protein, das die Resistenz von Pseudomonas-Bakterien gegen Antibiotika fördert. Das Verständnis der genauen Funktion des Proteins YgfB könnte neue Angriffspunkte für die medikamentöse Behandlung von Infektionen, die durch multiresistente Pseudomonas aeruginosa verursacht werden, bieten.

Pseudomonas aeruginosa ist ein Bakterium, das überall in der Umwelt vorkommt und sich gut an diese anpassen kann. Für gesunde Menschen ist der Kontakt mit P. aeruginosa meist ungefährlich. Für immungeschwächte Patienten kann dieses Bakterium jedoch zur Gefahr werden. Die Folge sind schwere Infektionen, z.B. der Atemwege, die auch mit Antibiotika nur schwer zu behandeln sind.
Forschende der Universität Tübingen und des Exzellenzclusters CMFI haben nun systematisch den Zusammenhang von bakteriellen Proteinen mit dem Abwehrmechanismus gegen Antibiotika untersucht, mit dem Ziel einen neuen Therapieansatz zu entwickeln. Die Ergebnisse der Studie wurden nun im Fachjournal Communications Biology von Nature veröffentlich.
Das Bakterium P. aeruginosa hat eine Strategie gegen Antibiotika
In der Therapie von bakteriellen Infektionen mit P. aeruginosa werden üblicherweise Zellwand oder Bakterien-DNA schädigende Antibiotika wie Ceftazidim oder Ciprofloxacin eingesetzt. Jedoch ist P. aeruginosa von Natur aus gegen eine Vielzahl von Antibiotika resistent. Zusätzlich ist ein Anstieg multi-resistenter Pseudomonas-Stämme zu beobachten, sodass Antibiotikatherapien immer seltener erfolgreich sind.
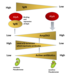
Ein wichtiger Abwehrmechanismus von P. aeruginosa gegen Antibiotika ist die Produktion des Enzyms β-Laktamase. Dieses Enzym zerstört Strukturen der β-Laktamantibiotika, wie Ceftazidim, und macht diese wirkungslos. Das Bakterium nimmt wahr, wenn seine Zellwand durch Antibiotika angegriffen und zerstört wird. Kommt es zu einer Zerstörung der Zellwand, entstehen Abbauprodukte (Anhyd-MurNAc-Peptide) die zu einer erhöhten Produktion von β-Laktamasen führen. Diese β-Laktamasen bauen Antibiotika ab. Die Antibiotika werden unwirksam, der Krankheitserreger überlebt und die Infektion kann sich weiter ausbreiten.
Ein Protein bestimmt über den Therapieerfolg
Das Forschungsteam um Erwin Bohn, Arbeitsgruppenleiter am Institut für Medizinische Mikrobiologie und Hygiene der Universitätsklinik Tübingen, suchte nun nach bakteriellen Proteinen, welche die Produktion von β-Laktamasen bei multiresistenten Pseudomonas-Bakterien beeinflussen. Das Team entdeckte das Protein YgfB, über dessen Funktion zuvor nichts bekannt war. Mit molekularbiologischen Methoden ist es den Forschenden gelungen zu klären, wie YgfB die Produktion von β-Laktamasen indirekt reguliert.
Das Protein YgfB interagiert nämlich mit dem Transkriptionsfaktor AlpA und hemmt auf diese Weise die von AlpA vermittelte Produktion des Enzyms AmpDh3. Dies ist ein entscheidender Schritt, denn das Enzym AmpDh3 würde sonst die Peptide der angegriffenen Bakterienzellwand (Anhyd-MurNAc) zerstören. In der Folge löst die größere Menge dieser Peptide eine erhöhte Produktion von β-Laktamasen aus. Die β-Laktamasen sind der entscheidende Faktor am Ende dieser Kaskade, welche die Bakterien unempfindlicher gegen Antibiotika wie Ceftazidim macht. Das Protein YgfB führt also indirekt zu Antibiotikaresistenzen bei Bakterien.
„Das Verständnis der Plastizität von Resistenzmechanismen ist wichtig, um sich an die wachsende Herausforderung der Multiresistenz bei Bakterien anzupassen und der erste Schritt zur Entwicklung neuer therapeutischer Optionen", sagt Erwin Bohn.
Aufbauend auf den Ergebnissen wollen die Forschenden versuchen, in die Abläufe einzugreifen, an denen YgfB beteiligt ist oder eine hohe AmpDh3-Produktion zu provozieren, um die β-Lactam-Resistenz zu brechen.
Original Publikation
Eggers O, Renschler FA, Michalek LA, Wackler N, Walter E, Smollich F, Klein K, Sonnabend MS, Egle V, Angelov A, Engesser C, Borisova M, Mayer C, Schütz M, Bohn E. YgfB increases β-lactam resistance in Pseudomonas aeruginosa by counteracting AlpA-mediated ampDh3 expression. Commun Biol 6, 254. (2023) doi: 10.1038/s42003-023-04609-4.
Dr. Khaled Selim
Interfakultäres Institut für Mikrobiologie und Infektionsmedizin
Auf der Morgenstelle 28
72076 Tübingen
Tel.: +49 7071 29-74627
E-Mail: khaled.selim@uni-tuebingen.de
Website
Leon Kokkoliadis
Medien- und Öffentlichkeitsarbeit
Tel: +49 7071 29-74707
E-Mail: leon.kokkoliadis@uni-tuebingen.de
Ähnliche Artikel



Science


The Independent



The Conversation

Inside CMFI Podcast



SWR Kultur

Deutschlandfunk Kultur

Inside CMFI Podcast




Inside CMFI Podcast

Tiny Matters Podcast



Inside CMFI Podcast

